| 产品名称 | 优尔金® 钙粉 |
| 备案人 | 陕西优利士乳业集团有限责任公司 |
| 备案人地址 | 陕西省咸阳市乾县杨汉工业园区 |
| 备案结论 | 按照《中华人民共和国食品安全法》《保健食品注册与备案管理办法》等法律、规章的规定,予以备案。 |
| 备案号 | 食健备G202561001461 |
| 附 件 | 1 产品说明书;2 产品技术要求 |
| 备 注 |
保健食品产品说明书
食健备G202561001461
────────────────────────────────────────
优尔金®钙粉
【原料】碳酸钙,酪蛋白磷酸肽
【辅料】乳粉,麦芽糊精,赤藓糖醇,抗坏血酸钠
【功效成分及含量】每袋含:钙320mg
【适宜人群】需要补充钙的4-17岁人群及成人
【不适宜人群】3岁以下人群及孕妇、乳母
【保健功能】补充钙
【食用量及食用方法】每日1次,每次1袋,食用方法:用温开水搅匀分散后服用。
【规格】5g/袋
【贮藏方法】本品须贮藏于阴凉干燥处,避免阳光暴晒或高温环境下存放。
【保质期】24个月
【注意事项】本品不能代替药物。适宜人群外的人群不推荐食用本产品。不宜超过推荐量或与同类营养素同时食用。
保健食品产品技术要求
食健备G202561001461
──────────────────────────
优尔金®钙粉
【原料】碳酸钙,酪蛋白磷酸肽
【辅料】乳粉,麦芽糊精,赤藓糖醇,抗坏血酸钠
【生产工艺】本品经混合、过筛、混合、过筛(14目)、包装等主要工艺加工制成。
【直接接触产品包装材料的种类、名称及标准】
直接接触产品包装材料“食品包装用复合膜”应符合《食品安全国家标准食品接触用塑料材料及制品》(GB4806.7-2023)的规定。
【感官要求】应符合表1的规定。
表1感官要求
| 项 目 | 指 标 |
| 色 泽 | 乳白色至乳黄色 |
| 滋味、气味 | 具有产品应有的气味和滋味,无异臭,无异味 |
| 状 态 | 应干燥、疏松、混合均匀、色泽一致,无正常视力可见外来异物 |
【鉴别】
无,本产品配方主要使用符合《保健食品原料目录(一)》规定的原料品种,控制项目均已列入功效成分指标进行检测控制,因此未制定鉴别项。
【理化指标】应符合表2的规定。
表2理化指标
| 项 目 | 指 标 | 检测方法 |
| 铅(以 Pb计),mg/kg | ≤2.0 | GB 5009.12 |
| 总砷(以 As计),mg/kg | ≤1.0 | GB 5009.11 |
| 总汞(以 Hg计),mg/kg | ≤0.3 | GB 5009.17 |
| 水分,% | ≤9.0 | GB 5009.3 |
| 灰分,% | ≤20.0 | GB 5009.4 |
| 酪蛋白磷酸肽,mg/5g | 16~64 | 附录A:酪蛋白磷酸肽的测定 |
| 粒度 | 粗粉 | 《中华人民共和国药典》 |
附录A:酪蛋白磷酸肽的测定
1、范围:
本方法适用于保健食品中酪蛋白磷酸肽的测定。
2、方法原理
试样用热水提取后,经C18反相色谱柱分离,以保留时间定性,外标法定量。
3、试剂和仪器设备要求
3.1试剂
3.1.1乙腈:色谱纯
3.1.2冰乙酸:分析纯
3.1.3酪蛋白磷酸肽标准品:酪蛋白磷酸肽原料
3.2仪器和设备
3.2.1天平,感量为0.1mg。
3.2.2超声波振荡器
3.2.3pH计:精度±0.01
3.2.40.45μm滤膜
3.2.5高效液相色谱仪,带有紫外检测器或二极管阵列检测器
3.3标准品
酪蛋白磷酸肽原料(酪蛋白磷酸肽含量以24.2%计,不同批次原料有差异,计算时以原料报告单为准)。
3.4标准溶液配制
3.4.1酪蛋白磷酸肽标准储备液(1mg/mL):准确称取酪蛋白磷酸肽原料0.396g,加水溶解并定容至100mL,临用前配制。
3.4.2酪蛋白磷酸肽标准工作液:分别准确吸取酪蛋白磷酸肽储备液1mL、2mL、4mL、8mL、16mL于50mL的容量瓶中,加水定容至刻度,混匀,得到浓度分别为20μg/mL、40μg/mL、80μg/mL、160μg/mL、200μg/mL的酪蛋白磷酸肽标准工作液,临用前配制。
4.实验分析步骤
4.1试样提取
称取混合均匀的试样约1.0g~5.0g(精确至0.1mg)于100mL锥形瓶中,加30mL约40℃的温水充分溶解试样,超声提取10min,冷却至室温,用10%乙酸溶液调试样溶液pH至4.6,转移至50mL容量瓶中并用水定容,滤纸过滤。滤液经0.45μm水相滤膜过滤后,即为试样待测液。
4.2色谱参考条件
4.2.1色谱柱C18反相色谱柱(粒径5μm,250mm×4.6mm)或具有同等性能的色谱柱
4.2.2柱温:28+1℃
4.2.3检测波长:280nm
4.2.4流动相:A:0.1%乙酸溶液,B:乙腈,梯度洗脱,0min-19min,2%B线性变换到50%B,19min-24min,50%B线性变换到95%B,24.1min-31min,保持2%B。
4.2.5流速:0.8mL/min
4.2.6进样量:30μL
4.3标准曲线的测定
将酪蛋白磷酸肽标准工作液依次进行色谱分析,以标准工作液浓度为横坐标,以峰面积为纵坐标,绘制标准曲线
4.4试样溶液的测定
将试样待测液进行色谱分析,测定峰面积,根据试样峰面积从标准曲线中查得相应的酪蛋白磷酸肽浓度
5.分析结果的表述
试样中酪蛋白磷酸肽含量计算:
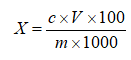
式中:
X——试样中酪蛋白磷酸肽的含量,单位为毫克每百克(mg/100g);
c——试样待测液中酪蛋白磷酸肽的浓度,单位为微克每毫升(μg/mL);
m——称样量,单位为克(g);
V——试样待测液最终的定容体积,单位为毫升(mL)。
计算结果保留小数点后一位。
6.精密度
重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。
7.其他
本方法检出限为4.5mg/100g,定量限为13.5mg/100g。
【微生物指标】应符合表3的规定。
表3微生物指标
| 项 目 | 指 标 | 检测方法 |
| 菌落总数,CFU/g | ≤10000 | GB 4789.2 |
| 大肠菌群,MPN/g | ≤0.92 | GB 4789.3 MPN 计数法 |
| 霉菌和酵母,CFU/g | ≤50 | GB 4789.15 |
| 金黄色葡萄球菌 | ≤0/25g | GB 4789.10 |
| 沙门氏菌 | ≤0/25g | GB 4789.4 |
【功效成分或标志性成分指标】应符合表4的规定。
表4功效成分或标志性成分指标
| 项 目 | 指 标 | 检测方法 |
| 每袋含 钙(以Ca计) | 250-400mg | GB 5009.92 第四法 |
【净含量及允许负偏差指标】
应符合JJF1070规定。
【原辅料质量要求】
1、碳酸钙:应符合GB1886.214《食品安全国家标准食品添加剂碳酸钙(包括轻质和重质碳酸钙)》的规定2、酪蛋白磷酸肽:应符合GB31617《食品安全国家标准食品营养强化剂酪蛋白磷酸肽》的规定3、乳粉:应符合GB19644食品安全国家标准乳粉的规定4、麦芽糊精:应符合GB15203食品安全国家标准淀粉糖的规定5、赤藓糖醇:应符合GB26404食品安全国家标准食品添加剂赤藓糖醇的规定6、抗坏血酸钠:应符合GB1886.44食品安全国家标准食品添加剂抗坏血酸钠的规定

